
- 首頁
-
CRO服務(wù)
 先導分子發(fā)現(xiàn)服務(wù)
先導分子發(fā)現(xiàn)服務(wù)
 抗體制備服務(wù)
抗體制備服務(wù)
 技術(shù)平臺
技術(shù)平臺
 技術(shù)優(yōu)化服務(wù)
技術(shù)優(yōu)化服務(wù)
- 產(chǎn)品中心
- BLOGS
- 研究成果
- 聯(lián)系我們
酵母展示技術(shù)最早是由美國的Boder和Wittrup于1997年提出,他們利用酵母表面展示的原理將外源蛋白質(zhì)插入到酵母表面的蛋白質(zhì)上,使其能夠在酵母表面表達出來。George P. Smith等人之后對該技術(shù)進行了改進,如在1998年,Smith等人報道了一種更簡便、高效的方法來構(gòu)建酵母表面展示的蛋白質(zhì)庫。隨著技術(shù)的不斷改進和完善,酵母展示技術(shù)已經(jīng)廣泛應(yīng)用于蛋白質(zhì)功能研究、藥物篩選、抗原鑒定、疫苗研發(fā)等領(lǐng)域。
酵母展示技術(shù)的原理
外源多肽、抗體或蛋白質(zhì)等通過與酵母表面展示系統(tǒng)中的蛋白質(zhì)進行融合表達,并使其在酵母表面高效地展示出來。該技術(shù)通常使用兩種酵母菌株:釀酒酵母(Saccharomyces cerevisiae)和畢赤酵母(Pichia pastoris)。釀酒酵母通常用于表達蛋白質(zhì)和抗體等,而畢赤酵母則更適合于表達復(fù)雜的糖基化蛋白質(zhì)。
常用的錨定蛋白有a-凝集素、Flo1p、Yps1p、Cwp2p、Sed1p、Pir1-4等(圖2)。展示的蛋白經(jīng)分泌途徑,首先被轉(zhuǎn)運到內(nèi)質(zhì)網(wǎng)腔內(nèi),然后從內(nèi)質(zhì)網(wǎng)轉(zhuǎn)運到高爾基體,最終錨定于細胞壁表面。
酵母展示系統(tǒng)繼承了噬菌體展示的表現(xiàn)型與基因型一致和易于擴增的特性,可根據(jù)編碼蛋白的特性對目的基因進行篩選。它不但可以應(yīng)用傳統(tǒng)的生物淘洗方法進行篩選,另外由于酵母細胞體積較大,從而決定了它在篩選方法上具有特殊優(yōu)勢:可用熒光激活細胞分選儀(fluorescence activated cell sorter,F(xiàn)ACS)進行篩選。具體過程如下:將展示文庫與靶分子一起孵育,表面表達有靶分子配體的酵母細胞就會與靶分子結(jié)合,洗去未結(jié)合的靶分子。隨后加入熒光標記的抗體,洗去游離的抗體分子。將熒光標記了的細胞懸液用FACS分選表達目的蛋白的酵母。
NBbiolab酵母表面展示平臺采用“α-凝集素”展示系統(tǒng),將納米抗體基因序列和表達標簽HA tag基因序列插入至蛋白質(zhì)支架-Aga2基因的展示質(zhì)粒載體中,該載體使用營養(yǎng)標記物在酵母中維持選擇性生長,并通過培養(yǎng)基中加入半乳糖誘導酵母進行表面展示,納米抗體融合蛋白被分泌并錨定在酵母細胞壁上。再結(jié)合磁珠及細胞分選技術(shù)進行多輪篩選,可篩選得到高親和力、高穩(wěn)定性的克隆。
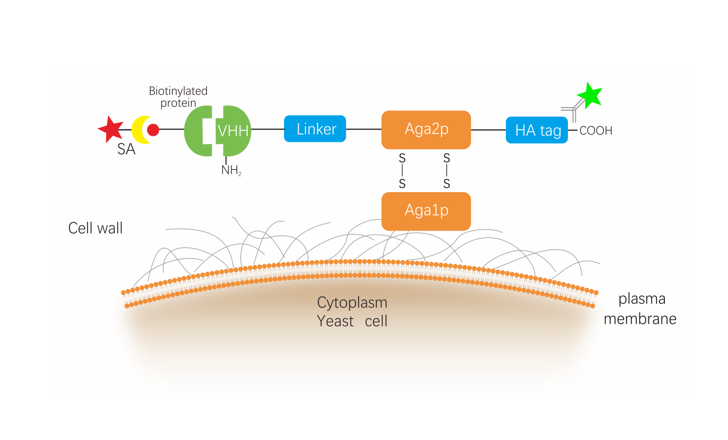
圖1 酵母表面展示原理
酵母表面展示技術(shù)優(yōu)勢
真核表達系統(tǒng):
酵母具有類似于高等真核生物的分泌途徑, 蛋白質(zhì)折疊在內(nèi)質(zhì)網(wǎng)中,其中伴侶蛋白,折疊酶和質(zhì)量控制機制確保僅分泌正確折疊的蛋白質(zhì)。
無偏向性:
酵母展示系統(tǒng)采用FACS分選技術(shù),基于抗體親和力及展示水平進行篩選,因此消除了表達引起的偏差,且能區(qū)分相差很小親和力的克隆。
精確控制篩選參數(shù):
酵母表面展示的篩選方法與流式細胞術(shù)提供的定量和多參數(shù)分析兼容。可對緩沖液組成、pH、溫度和抗原濃度等條件進行精確控制,實時了解展示水平及其抗原結(jié)合情況,分選在特定孵育條件下與靶蛋白結(jié)合的克隆。
基于抗體親和力及展示水平進行篩選:
通過使用多染色的 FACS,可以直接在酵母細胞表面上確定抗體親和力,從而無需耗時的亞克隆、表達和純化。
更高效獲得抗體序列:
抗體篩選速度快,3min即可完成10萬個細胞的分選,結(jié)合NGS可獲得上百條序列獨特的候選克隆。
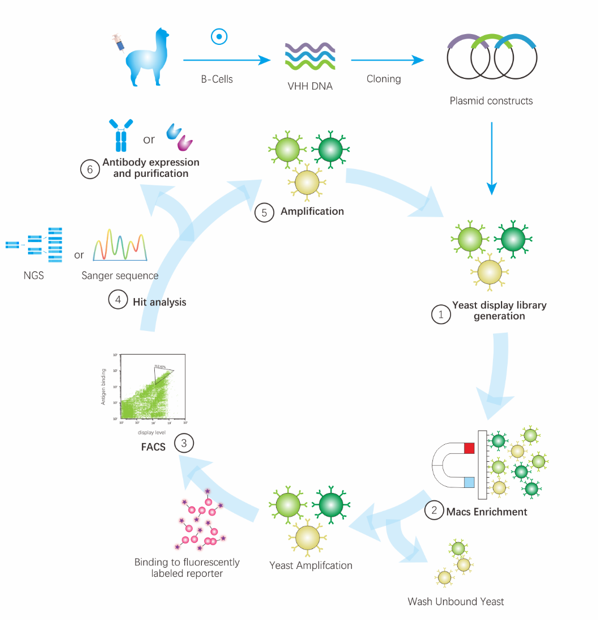
圖2 酵母展示納米抗體發(fā)現(xiàn)流程
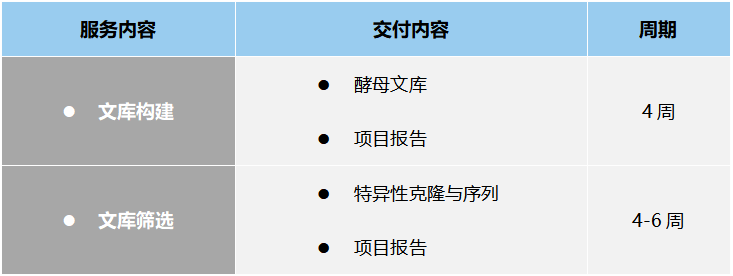
阿帕克生物酵母表面展示技術(shù)優(yōu)勢
1. 高質(zhì)量建庫表準,酵母庫容可達108。
2. 優(yōu)化信號肽,文庫表達率可達到65%~80%。
3. 與流式多色分選和NGS測序強力組合。
參考資料:
1. Chao G, Lau WL, Hackel BJ, et al. Isolating and engineering human antibodies using yeast surface display. Nature Protocols. 2006;1(2):755-768. doi:10.1038/nprot.2006.9.
2. Boder ET, Wittrup KD. Yeast surface display for screening combinatorial polypeptide libraries. Nature Biotechnology. 1997;15(6):553-557. doi:10.1038/nbt0697-553.
3. Bidlingmaier S, Liu B (2011) Construction of yeast surface-displayed cDNA libraries. Methods Mol Biol 729:199–210. doi: 10.1007/978-1-61779-065-2_13.
了解更多納米抗體相關(guān)內(nèi)容,可關(guān)注<阿帕克生物>微信公眾號,獲取最新資訊~
