
前言
G蛋白偶聯(lián)受體(GPCR)作為人體內(nèi)最大的膜蛋白超家族,調(diào)控著細(xì)胞對激素,神經(jīng)遞質(zhì)的大部分應(yīng)答,以及視覺,嗅覺,味覺等。GPCR在人體內(nèi)約有850個(gè)家族成員,其中一半被認(rèn)為是潛在的藥物靶點(diǎn)。目前FDA 批準(zhǔn)的藥物中至少有三分之一是針對 GPCR,其中小分子藥物占92%,多肽類藥物占5%,蛋白類藥物占2%,抗體藥有2款(Mogamulizumab 和 Erenumab)。據(jù)報(bào)道,目前上市的藥物中,前50種最暢銷的藥物20%就屬于G蛋白受體相關(guān)藥物,比如充血性心力衰竭藥物Coreg,高血壓藥物Cozaar,乳腺癌藥物Zoladex等等。盡管靶向GPCR的藥物開發(fā)歷史悠久,但其結(jié)構(gòu)的靈活性和不穩(wěn)定性,使得以GPCR作為靶點(diǎn)藥物的開發(fā)仍具有挑戰(zhàn)性。
GPCR結(jié)構(gòu)解析的難點(diǎn)
GPCR的三維結(jié)構(gòu)可以為以GPCR為靶點(diǎn)的藥物開發(fā)提供指導(dǎo),然而,相比與數(shù)目龐大的GPCR家族蛋白,迄今得到結(jié)構(gòu)解析的GPCR任占極少數(shù)。
GPCR結(jié)構(gòu)解析的難點(diǎn)在于[1],第一如何獲得大量的蛋白。晶體結(jié)構(gòu)解析需要毫克級別的蛋白,GPCR是7次跨膜蛋白,且部分GPCR在天然組織內(nèi)表達(dá)量低,難以通過傳統(tǒng)蛋白純化的方法獲得,而膜蛋白重組表達(dá)技術(shù)尚存諸多難點(diǎn),因此研究者們需要開發(fā)異源重組表達(dá)和純化的方法。第二如何穩(wěn)定受體的構(gòu)象。GPCR針對激素和神經(jīng)遞質(zhì)的信號感知與傳遞功能歸因于它們靈活多變的可塑性結(jié)構(gòu)。GPCR可以以多種功能上不同的構(gòu)象狀態(tài)存在。盡管這種結(jié)構(gòu)可塑性和動態(tài)行為對于GPCR功能是必需的,但是也成為獲得高分辨率穩(wěn)定狀態(tài)晶體結(jié)構(gòu)的障礙,而要獲得穩(wěn)定的活性狀態(tài)下的晶體結(jié)構(gòu)難度更大,這是因?yàn)闆]有G蛋白結(jié)合的GPCR活性構(gòu)象是極不穩(wěn)定性。
VHHs用于GPCR結(jié)構(gòu)解析
在GPCR結(jié)構(gòu)解析領(lǐng)域中做出杰出工作的科學(xué)家之一是來自美國斯坦福大學(xué)的Brian K. Kobilka教授。他也是ConfometRx的共同創(chuàng)辦人,一家專注于GPCR的生物技術(shù)公司。2011年Kobilka教授領(lǐng)導(dǎo)的國際研究團(tuán)隊(duì)報(bào)道了agonist-β2AR-Gs 三元復(fù)合體的詳細(xì)晶體結(jié)構(gòu),這一發(fā)現(xiàn)被稱為是一項(xiàng)真正具有突破意義的成果。因在β2AR受體上做出了突出貢獻(xiàn),Robert J. Lefkowitz 和 Brian K. Kobilka 于2012年被授予諾貝爾化學(xué)獎。
VHH Nb80鎖定GPCR的活性狀態(tài)構(gòu)象
β2AR是一類交感神經(jīng)系統(tǒng)的膜蛋白受體,利用內(nèi)源性兒茶酚胺如腎上腺素和去甲腎上腺素等激動劑參與人體許多生理和代謝過程。β2AR作為藥物靶點(diǎn),可用于哮喘、心血管等疾病的治療。因此,獲得β2AR晶體結(jié)構(gòu)顯得尤為重要。Kobilka研究小組與合作者一起在2007年連續(xù)發(fā)表了多篇β2AR的晶體結(jié)構(gòu)文章。但是這些結(jié)構(gòu)捕捉的都是β2AR結(jié)合拮抗劑的非激活狀態(tài)。
2011年,Kobilka研究小組應(yīng)用納米抗體技術(shù)才首次獲得活性狀態(tài)下的β2AR晶體結(jié)構(gòu)[2]。在這項(xiàng)研究工作中,Kobilka研究小組將純化的agonist-β2AR復(fù)合物以高密度包裝在磷脂載體中,以此為抗原免疫美洲駝,經(jīng)篩選得到結(jié)合特性類似于G蛋白的納米抗體Nb80,即結(jié)合激活狀態(tài)下的野生型β2AR和β2AR-T4L (β2AR-T4溶菌酶融合蛋白用于獲得高分辨率晶體結(jié)構(gòu))。
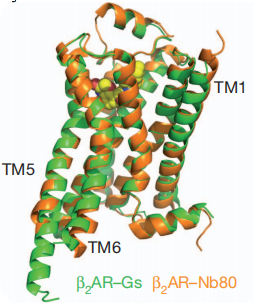
通過激動劑競爭性結(jié)合實(shí)驗(yàn),Kobilka研究小組檢測Gs(G蛋白異源三聚體)和Nb80對β2AR的激動劑親和力的影響。將β2AR蛋白包裝在HDL載體中,在沒有Gs或Nb80存在的情況下。 異丙腎上腺素(isoproterenol,β2AR的激動劑)的抑制常數(shù)(Ki)為107 nM。有Gs存在的情況下,有兩種親和力狀態(tài),因?yàn)椴⒎撬械摩?AR都與Gs結(jié)合(除了經(jīng)典的G蛋白信號傳遞途徑,目前GPCR公認(rèn)的信號傳導(dǎo)途徑還有β-arrestin依賴性的信號傳導(dǎo)途徑)。在Gs結(jié)合狀態(tài)下,異丙腎上腺素對受體β2AR的親和力增加100倍(Ki = 1.07 nM)(圖1D)。同樣地,在Nb80結(jié)合β2AR的情況下,異丙腎上腺素對受體β2AR的親和力增加了95倍(Ki =1.13 nM)(圖1E)。相反,Nb80對β2AR與反向激動劑ICI-11的結(jié)合沒有什么影響。這些結(jié)合數(shù)據(jù)表明,Nb80結(jié)合β2AR后形成的穩(wěn)定活性構(gòu)象與通過Gs穩(wěn)定的構(gòu)象非常相似,Nb80完美地模仿再現(xiàn)了agonist-GPCR-Gs的三元復(fù)合體模型,證明其具有與Gs蛋白類似的功能。不僅如此,Kobilka研究小組同年發(fā)表的另一篇文章中[3],從Gs和Nb80分別結(jié)合的β2AR晶體結(jié)構(gòu)對比圖(圖2)能夠看出,二者各自結(jié)合β2AR后所捕獲的β2AR活性構(gòu)象僅有略微的差別。
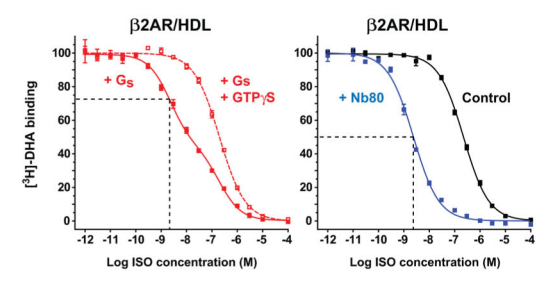
圖1. Gs(the stimulatory G protein)和Nb80對β2AR的激動劑親和力的影響。
接著,研究者將Nb80-β2AR與小分子完全激動劑BI-167107結(jié)合,在脂立方相( Lipidic cubic phase,LCP) 中獲得有活性的3. 5?分辨率的 β2AR-T4L-NB80 復(fù)合物晶體結(jié)構(gòu)(圖3)。從晶體結(jié)構(gòu)中可以看到Nb80與β2AR的胞質(zhì)端結(jié)合,并且Nb80的CDR3 loop伸向β2AR的核心部位。活性構(gòu)象的β2AR-T4L-Nb80與失活狀態(tài)的β2AR質(zhì)端向外移動11?以及跨膜段5(TM5)和跨膜段7(TM7)的重新排列有關(guān),這與在視蛋白o(hù)psin(一種活性形式的視紫紅質(zhì))中觀察到的非常相似。通過納米抗體Nb80捕獲到活性狀態(tài)下β2AR的晶體結(jié)構(gòu)加深了我們對激動劑結(jié)合和激活過程的了解。
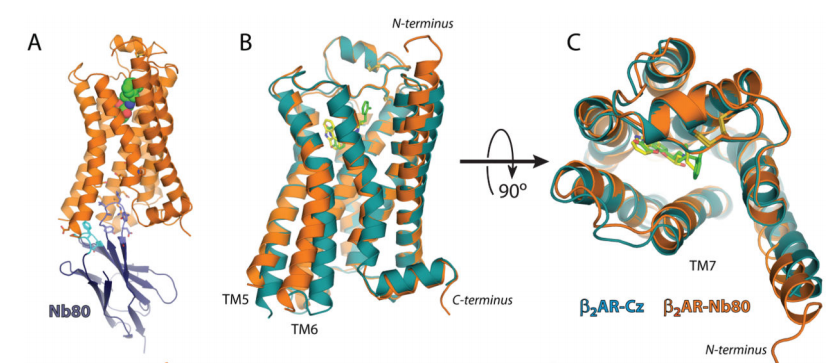
圖3. 激動劑-Nb80穩(wěn)定的活化β2AR晶體結(jié)構(gòu)與反向激動劑結(jié)合的β2AR的比較
反向激動劑Carazolol(黃色)與β2AR-T4L結(jié)合的結(jié)構(gòu)(β2AR-Cz) 顯示為藍(lán)色。激動劑BI-167107(綠色)與Nb80穩(wěn)定的β2AR-T4L結(jié)合的結(jié)構(gòu) (β2AR-Nb80)顯示為橙色。將這兩個(gè)結(jié)構(gòu)經(jīng)Pymol align進(jìn)行對比。
A.β2AR-Nb80復(fù)合物的側(cè)視圖,Nb80的CDR1(淺藍(lán)色)和CDR3(藍(lán)色)。
B.兩種復(fù)合物結(jié)構(gòu)疊加的側(cè)視圖,顯示出受體β2AR的胞內(nèi)部分(G蛋白結(jié)合域)結(jié)構(gòu)比較有顯著的變化。
C.受體β2AR的胞外部分(配體結(jié)合域)的比較,顯示結(jié)構(gòu)變化不大。
VHH Nb35穩(wěn)定GPCR-Gs的結(jié)合構(gòu)象
Kobilka研究小組在2011年報(bào)道的另外一份重磅研究成果,β2AR-Gs的晶體結(jié)構(gòu)[3],同樣采用了納米抗體來穩(wěn)定復(fù)合物的構(gòu)象,不同與Nb80(模擬G蛋白結(jié)合GPCR),這項(xiàng)研究中用到的納米抗體Nb35用于結(jié)合G蛋白異源三聚體(Gs),穩(wěn)定β2AR-Gs復(fù)合物。從獲得的3. 2?分辨率的T4L-β2AR–Gs–Nb35復(fù)合物晶體結(jié)構(gòu)中觀察到(圖4),Nb35插入在Gα亞基和Gβ亞基的交匯面,其CDR1 loop與Gβ亞基相互作用,較長的CDR3 loop則同時(shí)與Gα亞基和Gβ亞基相互作用,并且Nb35的框架區(qū)也與相鄰的Gα亞基發(fā)生相互作用。
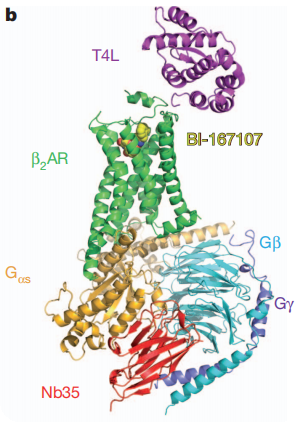
圖4. T4L-β2AR–Gs–Nb35整體結(jié)構(gòu)顯示β2AR(綠色)與激動劑BI-167107(黃色)結(jié)合并與Gα橙色大面積結(jié)合。Gα與Gβ(青色)和Gγ一起(紫色)構(gòu)成G蛋白異源三聚體(Gs).
Nb35參與捕獲的β2AR–Gs復(fù)合晶體結(jié)構(gòu)是GPCR跨膜信號傳導(dǎo)的第一個(gè)高分辨率視圖,為GPCR:G蛋白復(fù)合物的形成,GTP結(jié)合以及復(fù)合物解離過程中的機(jī)制研究提供了重要的框架。深入了解GPCR:G蛋白活化的結(jié)構(gòu)基礎(chǔ)將為藥物發(fā)現(xiàn)提供新的可行方法。繼這篇重磅研究之后,Kobilka教授接著對β2AR多種狀態(tài)做了構(gòu)效關(guān)系的研究。除此之外,通過類似的思路,他們還對GPCR B類受體等蛋白做了結(jié)構(gòu)解析。2014年,Kobilka教授實(shí)驗(yàn)室發(fā)表綜述,總結(jié)了用于穩(wěn)定GPCR蛋白構(gòu)象的納米抗體的篩選流程[4]。
VHHs將GPCR鎖定在可成藥構(gòu)象中加速靶向藥物發(fā)現(xiàn)
隨著β2AR多種狀態(tài)下的晶體結(jié)構(gòu)的成功捕獲,在促進(jìn)人們對GPCR參與信號傳導(dǎo)機(jī)制理解的同時(shí),富有想法的科學(xué)家們延續(xù)納米抗體在GPCR研究領(lǐng)域的優(yōu)勢,并將其發(fā)展為靶向GPCR的藥物發(fā)現(xiàn)關(guān)鍵平臺之一。比如Confo Therapeutics公司,人員組成中不僅擁有多位Ablynx前員工,也包含參與2011年β2AR結(jié)構(gòu)解析工作的科學(xué)家。
Confo Therapeutics公司核心技術(shù)平臺設(shè)計(jì)的原理是使用VHHs將GPCR以及GPCR:Gs信號轉(zhuǎn)到復(fù)合物穩(wěn)定在與疾病相關(guān)的藥理構(gòu)象狀態(tài),進(jìn)而篩選出更具選擇性和有效性的候選藥物分子。該公司將可穩(wěn)定構(gòu)象的VHHs統(tǒng)一命名為ConfoBodies(簡稱Cbs),并分為三類[5]。I型Cbs是模擬G蛋白的VHHs,它直接與激活的GPCR的胞內(nèi)環(huán)相互作用,穩(wěn)定活性構(gòu)象(圖5,A)。II型Cbs是直接與非活化的GPCR的胞內(nèi)環(huán)結(jié)合并穩(wěn)定非活性構(gòu)象。III型Cbs是穩(wěn)定GPCR:Gs信號轉(zhuǎn)到復(fù)合物的VHHs,通過與Gs信號蛋白相互作用,間接穩(wěn)定GPCR:Gs信號轉(zhuǎn)到復(fù)合物的活性構(gòu)象(圖5,B)。
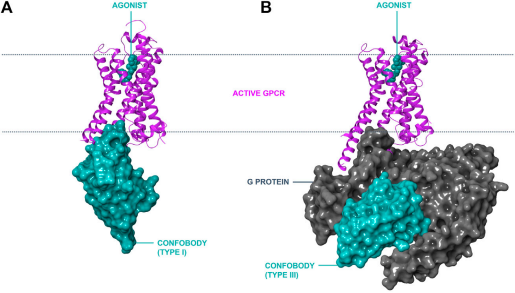
圖5. ConfoBodies(Cbs)的作用模式圖。
2018年Jan Steyaert研究小組 (2011年β2AR晶體結(jié)構(gòu)解析工作的作者之一)發(fā)表的文章也展示了這種基于VHHs的藥物發(fā)現(xiàn)設(shè)計(jì)[6]。在放射性配體競爭實(shí)驗(yàn)中,研究者對比活性構(gòu)象的β2AR-Nb80復(fù)合物相對于基礎(chǔ)活性構(gòu)象 (basal activity)的β2AR-Nbirr對激動劑小分子和拮抗劑小分子與受體β2AR親和力的差異(圖6)。結(jié)果顯示,G蛋白模擬物Nb80 有效地將β2AR鎖定在活性狀態(tài)構(gòu)象(圖6 A)。
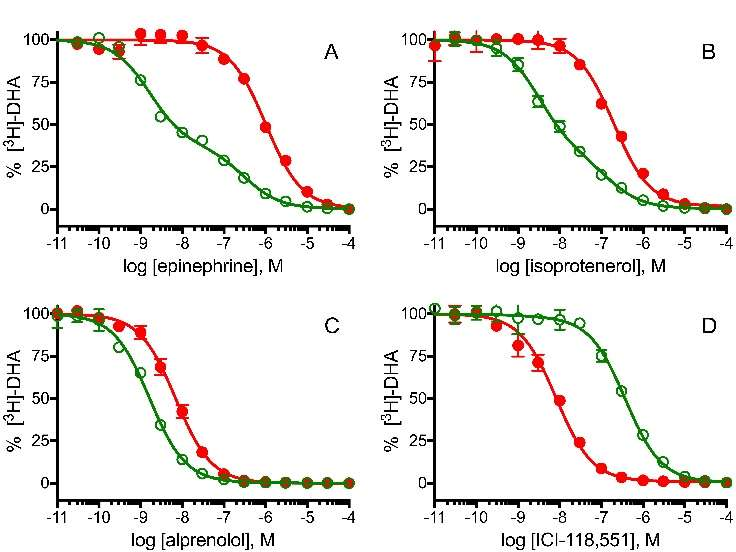
圖6. 放射性配體競爭實(shí)驗(yàn)。激動劑、拮抗劑和反激動劑不同程度地取代了放射性標(biāo)記的拮抗劑[3H]-二氫腎上腺素([3H]-DHA)結(jié)合到受體的原始狀態(tài)(β2AR-Nbirr,closed red symbols)和活性狀態(tài)(β2AR-Nb80,open green symbols)。
(a)-(b) β2AR與Nb80結(jié)合將受體β2AR穩(wěn)定在高親和力的活性狀態(tài),與原始狀態(tài)(β2AR-Nbirr)相比,β2AR-Nb80對配體Epinephrine(腎上腺素)和Isoprotenerol(異丙腎上腺素)的結(jié)合強(qiáng)度提高約2000倍。
(c) Alprenonol(丙烯醇),一種中性拮抗劑,與β2AR-Nb80和β2AR-Nbirr的結(jié)合強(qiáng)度相當(dāng)。
(d) β2AR反向激動劑如ICI-118,551優(yōu)先結(jié)合受體的基礎(chǔ)狀態(tài),而不是活性狀態(tài)。
通過這種便捷的設(shè)計(jì),研究者在納米抗體的參與下將受體β2AR穩(wěn)定在活性或基礎(chǔ)構(gòu)象狀態(tài)下,然后測量配體結(jié)合親和力的變化,可用于對多種新型激動劑進(jìn)行鑒定和排序,并可進(jìn)行激動劑、拮抗劑或反激動劑的功效分類。緊接著Jan Steyaert研究小組通過單點(diǎn)放射性配體置換試驗(yàn),對1000個(gè)小分子(分子量在80-300 Da且少于三個(gè)氫鍵供體或受體的小分子)進(jìn)行篩選,檢測它們與受體的激活狀態(tài)(β2AR-Nb80復(fù)合物)和基礎(chǔ)狀態(tài)(β2AR-Nbirr復(fù)合物)的結(jié)合(圖7)。經(jīng)這種比較篩選,發(fā)現(xiàn)了大量的片段優(yōu)先結(jié)合活性狀態(tài)的受體(β2AR-Nb80復(fù)合物),表現(xiàn)出與β2AR激動劑類似的結(jié)合特性。而其他與β2AR-Nb80和β2AR-Nbirr的結(jié)合強(qiáng)度相當(dāng)?shù)男》肿樱騼?yōu)先結(jié)合基礎(chǔ)活性狀態(tài)的小分子,則分別類似于拮抗劑或反向激動劑。
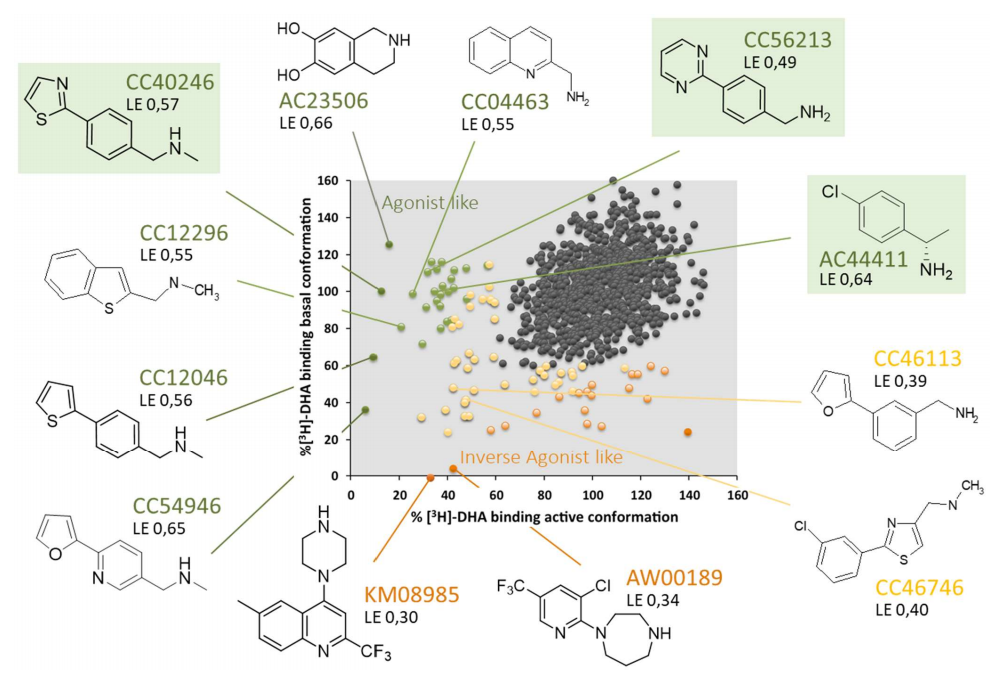
圖7. 對β2AR的激活態(tài)和基礎(chǔ)態(tài)進(jìn)行基于小分子片段的比較篩選。每個(gè)點(diǎn)測量的是放射性配體([3H]-DHA)在受體激活狀上的剩余結(jié)合(X軸),與受體基礎(chǔ)狀(Y軸)上的剩余結(jié)合。綠色突出顯示的小分子被選中進(jìn)行表征。
接下來研究者從高選擇性結(jié)合激活態(tài)β2AR的小分子中選出3個(gè)(CC40246、CC56213和AC44411)用于評估這種生化篩選特定分子片段的方法是否可以作為設(shè)計(jì)強(qiáng)效激動劑的起點(diǎn)。為了實(shí)現(xiàn)結(jié)構(gòu)的多樣性和覆蓋不同的拓?fù)鋵W(xué)和化學(xué)空間,在計(jì)算工具的幫助下,基于選定的小分子,研究者設(shè)計(jì)出一組衍生的小分子化合物(文獻(xiàn)6補(bǔ)充材料)并進(jìn)行功能評估(圖8)。
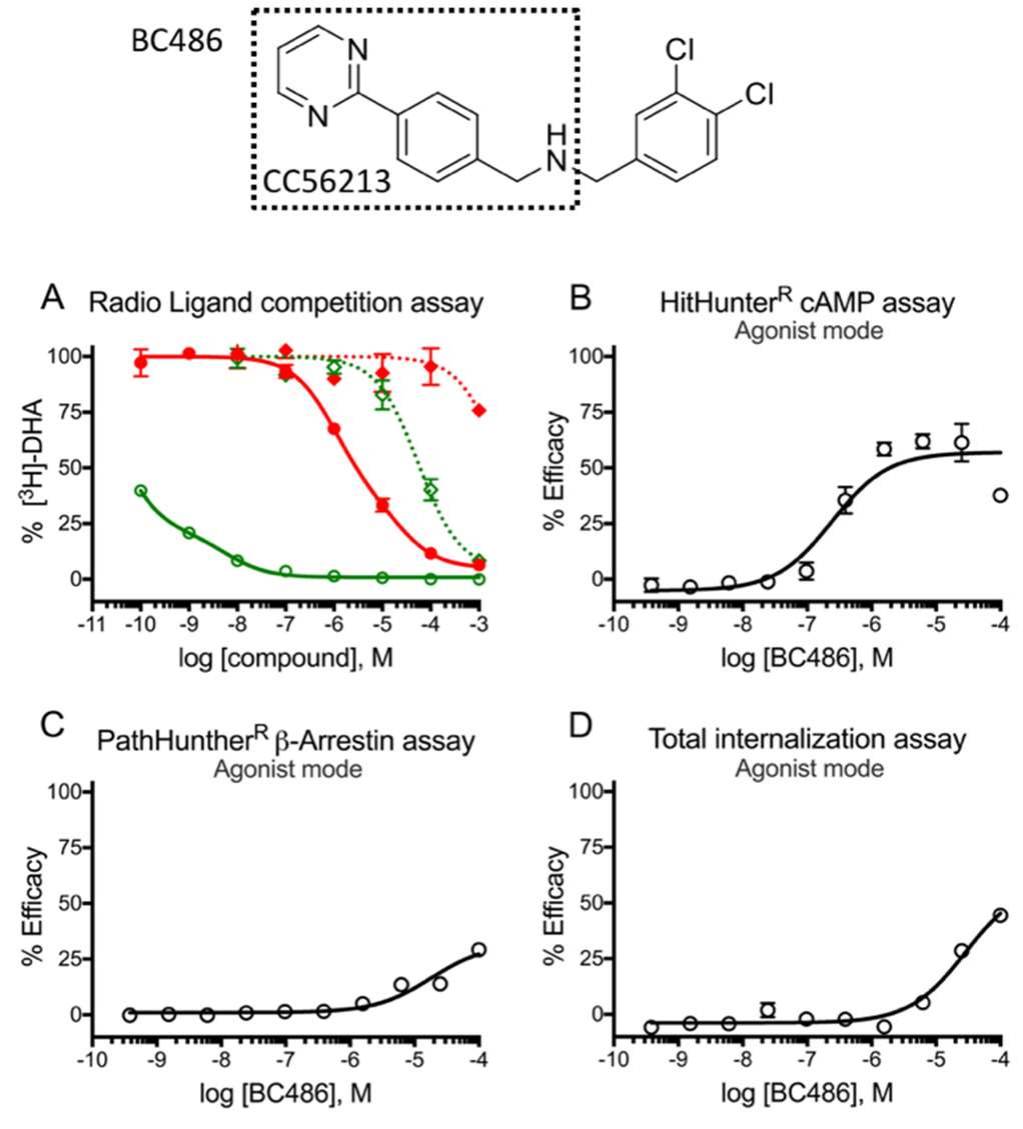
圖8. 基于CC56213設(shè)計(jì)的代表性衍生化合物BC486的功能評估。放射性配體競爭實(shí)驗(yàn)和三個(gè)激動劑模式下的細(xì)胞試驗(yàn)。
(a) 在使用放射性[3H]-DHA示蹤劑的配體競爭實(shí)驗(yàn)中 BC486(circle)與設(shè)計(jì)它所參考的原始化合物CC56213(diamonds)功能相似,都是優(yōu)先結(jié)合激活狀態(tài)的β2AR-Nb80(綠色曲線)而不是基礎(chǔ)狀態(tài)的β2AR-Nbirr(紅色曲線)。
(b) β2AR HitHunther cAMP assay檢測 BC486誘導(dǎo)的cAMP積累
(c) β2AR PathHuntherβarrestin assay檢測BC486引起的βarrestin的招募。
(d) PathHunter? Activated GPCR Internalization assay檢測BC486引起的β2AR內(nèi)吞。
功能實(shí)驗(yàn)顯示選出的高親和力的片段衍生化合物對 β2AR-Nb80 表現(xiàn)出pM親和力并且區(qū)分激活狀態(tài)與基礎(chǔ)狀態(tài)的親和力相差四個(gè)數(shù)量級,接近β2AR受體的全動態(tài)激活。這些片段衍生的化合物在細(xì)胞測定中也都展示出相似的功能。
小結(jié)
GPCR作為生物體中表達(dá)和功能最廣泛的一類蛋白,是重要的藥物靶點(diǎn)。在GPCR結(jié)構(gòu)解析和信號傳導(dǎo)機(jī)制研究工作中,納米抗體技術(shù)的應(yīng)用起到至關(guān)重要的作用,納米抗體捕獲GPCR的功能構(gòu)象狀態(tài)、特別是其活性構(gòu)象狀態(tài),從而允許對GPCR進(jìn)行結(jié)構(gòu)和功能分析,包括高分辨率結(jié)構(gòu)分析和由其衍生的許多其他應(yīng)用。目前,已有多個(gè)研究團(tuán)隊(duì)將納米抗體用于建立構(gòu)象選擇性片段的靶向GPCR的候選分子篩選分析和發(fā)現(xiàn),以從中得到具有理想的體外藥理學(xué)和效力的分子。納米抗體成為擴(kuò)展藥物發(fā)現(xiàn)的工具箱,將大力促進(jìn)GPCR靶向性的新結(jié)構(gòu)藥物的開發(fā)。
參考資料:
[1]. https://fanpusci.blog.caixin.com/archives/252858
[2]. Rasmussen. et al. Structure of a nanobody-stabilized active state of the β2 adrenoceptor.
Nature 469, 175–180 (2011). https://doi.org/10.1038/nature09648
[3]. Rasmussen. et al. Crystal structure of the β2 adrenergic receptor–Gs protein complex.
Nature 477, 549–555 (2011). https://doi.org/10.1038/nature10361
[4]. Pardon, E., Laeremans, T., Triest, S. et al. A general protocol for the generation of Nanobodies for structural biology.
Nat Protoc 9, 674–693 (2014). https://doi.org/10.1038/nprot.2014.039
[5]. Laeremans T. et al. Accelerating GPCR Drug Discovery With Conformation-Stabilizing VHHs. Front. Mol. Biosci. 9:863099(2022). doi: 10.3389/fmolb.2022.863099
[6]. Pardon, Els. et al. Nanobody-Enabled Reverse Pharmacology on G-Protein-Coupled Receptors. Angewandte Chemie (International ed. in English) vol. 57,19 (2018): 5292-5295. doi:10.1002/anie.201712581
了解更多納米抗體相關(guān)內(nèi)容,可關(guān)注<阿帕克生物>微信公眾號,獲取最新資訊~


