前言
隨著單分子定位的超分辨率顯微鏡的最新發(fā)展,在低于衍射極限的分辨率下,對細胞結構成像已經(jīng)成為一種廣泛的技術。納米抗體的小尺寸、易于生產和基因工程使其成為生物醫(yī)學成像和分子治療的很有前途的應用工具。已經(jīng)有許多研究證實了將納米抗體帶上標簽后,可以用作納米級的檢測工具。例如,針對GFP和RFP等熒光蛋白的納米抗體,在標記上有機染料后可用于細胞骨架成分的超分辨率顯微鏡成像。本文將為大家介紹納米抗體在單分子定位的超分辨率顯微鏡中的技術應用。
傳統(tǒng)有機染料在熒光顯微成像中的局限
近年來,隨著一些突破性的熒光超分辨率成像方法的發(fā)展,光學分辨率的極限已被降低到幾納米。其中,單分子定位顯微鏡(single-molecule localization microscopy,SMLM)技術已經(jīng)能夠以前所未有的分辨率對熒光標記的特征進行展示,并且越來越多地用于解釋亞細胞的組織結構。
熒光顯微鏡由于相對簡單和快速的樣品制備、顯著的對比度和高度的特異性,在可視化生物分子相互作用上具備巨大潛力。然而,由于SMLM技術的性質決定了SMLM需要特定、有效的明亮的熒光團輸送到目標結構的近距離,而不增加過多的背景。
在傳統(tǒng)的間接免疫熒光法中,染料可以通過抗體來傳遞,目標表位用一抗修飾,然后用熒光標記的二抗檢測,但是它們的大尺寸(約12-15 nm)會使染料和表位之間產生約10nM的"連接誤差",因此降低了超分辨率熒光顯微鏡可實現(xiàn)的蛋白質定位精度和準確性。而且高度特異的抗體只適用于某些特定蛋白質。基于光活化熒光蛋白或酶標記方案的方法則需要生產新的融合構建體,但這些構建體需要被定性,而最終結果可能沒有功能活性。同時由于SMLM依賴于數(shù)千個單個分子的分辨率,其限制因素是目標分子的標記成功率。雖然現(xiàn)有的熒光團如Alexa Fluor 647(AF647)提供了足夠的光子用于樣品中染料定位的高精度,但最終圖像是否能準確地表征目標結構在很大程度上取決于其遞送的效率和準確性。如果染料沒有被輸送到目標結構附近或與細胞結構非特異性結合,則會導致顯著的畸變。
納米抗體在細胞超微結構研究中的應用及優(yōu)勢
相比于使用全長抗體傳遞有機染料的熒光成像傳統(tǒng)方法,體積更小的納米抗體介導的有機染料靶向目標分子,既保有目標特異性和高親和力,也具備最小的連接誤差。
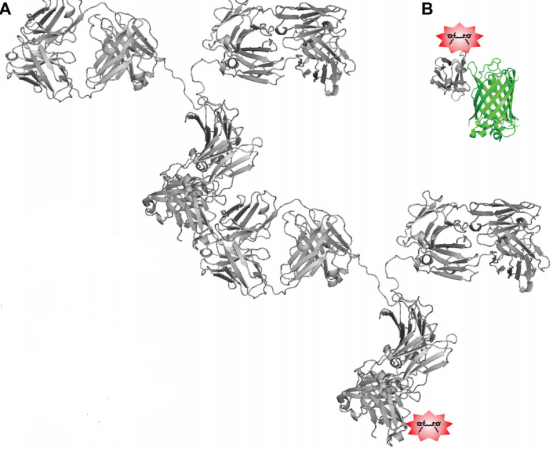
圖1 . 將有機染料輸送到目標結構上的方法。
A.熒光團通過用目標特異性一抗和二級標記抗體進行間接標記來將熒光團傳遞到目標結構的。
B.熒光團與一個高度特異性的抗GFP納米抗體的結合,使染料更接近GFP基因標記的目標結構。
1. 納米抗體增加在標記結構中的標記密度和分辨率
研究者使用不同的免疫熒光法觀察細胞環(huán)境中密集多組分組件的成像。核孔復合體(NPC)是一種高度排列的圓柱形多蛋白結構,分子量110 MDa,外徑為120nm。這種超大尺寸對任何結構和功能研究都構成了巨大挑戰(zhàn)。研究者使用EGFP標記核孔蛋白Nup43,并通過AF647標記的抗GFP納米抗體進行SMLM成像。可以在固定細胞的細胞核下表面看到直徑為100nm的環(huán)狀結構,這與Nup43 的預測位置一致(圖.2A )。在某些情況下,甚至可以觀察到中央旋轉的八倍對稱排列。而傳統(tǒng)的間接免疫熒光法(一抗GFP抗體和二抗小鼠抗體)觀察Nup43-EGFP(圖.2B) 的圖像雖然包含NPC的定位,但幾乎不能觀察到完整的環(huán)形結構,可能原因是由于在核孔復合體的密集環(huán)境中,相對較大的抗體標記形成了一定的的空間位阻。因此,小體積的納米抗體在擁擠的細胞環(huán)境中可提供優(yōu)越的表位可及性。
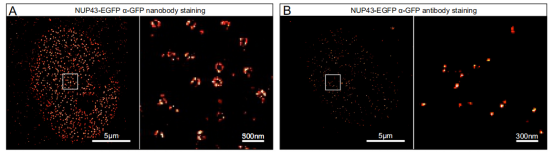
圖2.納米抗體和全長抗體標記核孔復合體的表位可及性差異比較。圖像顯示了穩(wěn)定表達Nup43-EGFP的固定U2OS細胞,其細胞核的下表面。
A.Nup43-EGFP通過AF647偶聯(lián)的抗GFP納米抗體進行標記。
B.Nup43-EGFP標記為一抗GFP抗體和AF647偶聯(lián)二抗抗體。
2. 納米抗體的小尺寸可提高標記中的最小分辨率
研究者使用三種不同的策略標記小窩(caveolae),這是由膜相關蛋白 Caveolin 1(Cav1)形成的穴樣內陷。首先,使用抗Cav1一抗和AF647標記的二抗來檢測大鼠上皮細胞NRK52E細胞中的小窩。當進行SMLM測量時,能夠將固定細胞膜上的Cav1組件可視化為平均直徑116nm的環(huán),這是膜平面上一個空心杯狀凹窩的二維投影(圖.3C)。接下來,在NRK52E細胞中瞬時過表達Cav1-EGFP,并使用AF647-抗GFP納米抗體進行標記,在重建的SMLM圖像中看到的小窩形態(tài)與圖3C相同,但直徑更小,為94nm。(圖.3D ) 。同時對瞬時轉染Cav1-PAmCherry的HeLa細胞的小窩進行了SMLM成像。在重建的SMLM圖像中,小窩表現(xiàn)為直徑為128nm的點云,僅在少數(shù)情況下可見結構呈環(huán)狀(圖.3E )。雖然PAFP基因標記具有較高的標記效率和特異性,三種比較標記方法的連鎖誤差最小,但PAmCherry的光子產率比AF647低4-5倍,導致定位精度大約低兩倍。上述的觀察結果證明納米抗體標記允許在SMLM測量中分辨出更精細的細節(jié)。
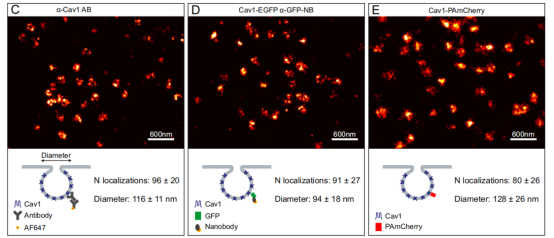
圖3. (C-E)使用不同的標記策略獲得的固定細胞基底膜上的小窩的超分辨率圖像。
C.通過兔抗Cav1抗體和二級AF647偶聯(lián)抗體標記的NRK52E細胞中的小窩。
D.Cav1-EGFP在用AF647-抗GFP納米抗體標記的NRK52E細胞中瞬時表達。
E.HeLa細胞中Cav1-PAmCherry的PALM圖像。
3.雙色納米抗體可在SMLM進行準確的共定位分析
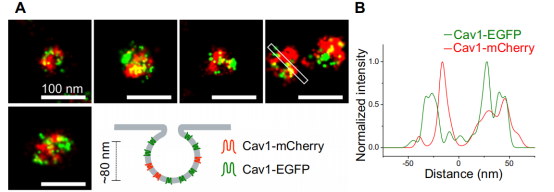
使用納米抗體進行雙色SMLM,這種方法為兩種顏色都提供了高分辨率,最小限度地減少了串擾,并且沒有色差,總體上允許在SMLM 中進行非常準確的共定位分析。研究者對固定細胞質膜上的小窩進行了雙色成像,通過觀察多蛋白結構的兩個不同組分證明納米抗體標記的質量。用Cav1-EGFP和Cav1-mCherry共轉染人U2OS細胞,用AF647-anti-GFP和CF680-anti-RFP納米抗體進行標記。重建的SMLM圖像顯示與預期的一樣,這兩種融合蛋白在小窩內幾十納米的尺度上共定位,顯示出了它們的詳細形態(tài)(圖4.A )。此外,圖像還能夠分辨出兩種顏色的凹窩的空心環(huán)狀投影,因為在兩個通道的橫向輪廓中都可以檢測到兩個間隔小于50nm的峰(圖,4B ) 。
接下來,研究者挑戰(zhàn)了兩個緊密間隔、內化小窩形態(tài)成分不同的可視化。Dynamin2是一種GTPase,與小窩結合,作為成熟小窩頸部的裂變環(huán),從質膜內化形成胞質囊泡。Dynamin2的顯性負性形式Dyn2K44A是一個不能結合GTP的突變體,抑制小泡裂變,并在質膜上阻止小泡的成熟。Dyn2K44A聚集在不完全收縮的小窩頸部周圍。在U2OS細胞中瞬時共表達Cav1-mCherry和Dyn2K44A-EGFP,固定細胞,用AF647-Anti-GFP和Cf680-Anti-RFP納米抗體標記,可以通過SMLM成像清楚地觀察Dyn2K44A-EGFP定位與Cav1-mcherry陽性結構的關聯(lián),并發(fā)現(xiàn)Dyn2K44A-EGFP染色位于小窩中心的離散點(圖.5) 。因此,在單個小窩的側面輪廓中,Dyn2K44A-EGFP染色顯示在Cav1-mCherry的兩個峰之間的單峰(圖.5)。
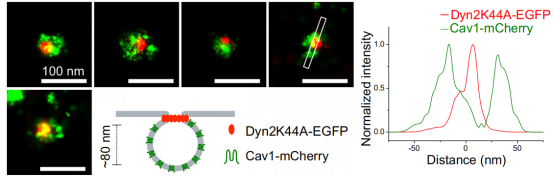
圖5.Cav1-mCherry和Dyn2K44A-EGFP的SMLM成像左.兩幅包含Cav1-mCherry(綠色)和Dyn2K44A-EGFP(紅色)的單個小窩的彩色圖像,以及Cav1-mCherry(綠色)在小泡膜上的相對定位和Dyn2K44A-EGFP(紅色)的示意圖。右.Cav1-mCherry(綠色)和Dyn2K44A-EGFP(紅色)的強度曲線顯示為以Cav1的兩個峰為中心的單峰。
4. 單顆粒示蹤(Single particle tracking,SPT)
雖然溶質和膜的結合擴散到特殊形狀的刺突被廣泛研究,但是這種擴散是如何調節(jié)的目前還不完全清楚。如果使用帶有染料的納米抗體標記細胞膜上的目標蛋白,而目標蛋白空間位置可以隨著時間的推移以納米精度確定,這樣,跨膜蛋白的運動就可以在單分子水平上進行定量描述。基于這樣的構思,研究者利用納米抗體動態(tài)研究神經(jīng)元樹突軸(<2um)蘑菇狀突起。研究者在培養(yǎng)的海馬神經(jīng)元的單個刺突中,首先對膜相關的CD4-mRFP進行光漂白(FRAP)實驗后的熒光恢復(圖.6A和B)。然后,使用Atto647N-anti-RFP納米抗體進行單顆粒示蹤,通過單分子水平的實驗補充了這種整體擴散測量(圖.6 C )。
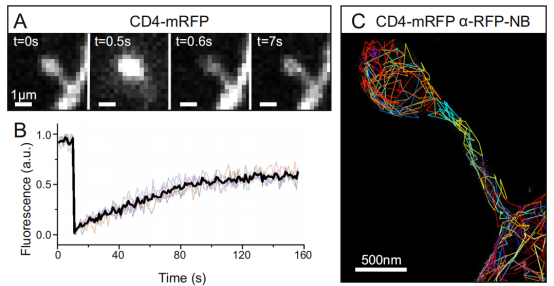
圖6. 結合光漂白后的熒光恢復(FRAP)技術和單粒子對表達CD4-mRFP的海馬神經(jīng)元樹突棘的跟蹤測量。
A.在FRAP實驗中記錄的圖像序列的單幀顯示。
B.連續(xù)5次FRAP實驗獲得的彩色熒光恢復曲線和平均值(黑色)。
C.在SPT過程中通過Atto647N-anti-RFP納米抗體與(A)對應的樹突棘上獲得的單分子軌道。
5. 納米抗體用于監(jiān)測兩種不同類型的膜相關分子的橫向遷移率
研究者在大鼠內皮NRK52E細胞的質膜中使用L-mHoneydewGT46和GPI-EGFP進行雙色單顆粒示蹤觀察[2]。EGFP通過GPI錨定在質膜上,而L-mHoneydew-GT46是單次跨膜蛋白。mHoneydew是dsRed的一種黃色熒光衍生物,可被抗RFP納米抗體識別。由于EGFP和mHoneydew都在光譜的綠黃色區(qū)域發(fā)射,可以使用橙紅色Alexa Fluor 555(AF555)和遠紅色Atto647N的染料。這兩種染料都具有優(yōu)良的量子產率和高光穩(wěn)定性,因此非常適合于單顆粒示蹤,二者的發(fā)射光可以用二向分色鏡進行光譜分離。當將AF555-anti-RFP和Atto647N-anti-GFP納米抗體以亞納摩爾濃度添加到成像緩沖液中時,研究者能夠同時追蹤它們在雙轉染細胞的基底膜上的運動(圖.7D )。利用此方法,直接對雙色單顆粒進行示蹤,在一個實驗中為兩個分子產生了數(shù)百個軌跡,并清楚地檢測到脂錨定和跨膜分子的膜運動的差異(圖.7E和7F)。
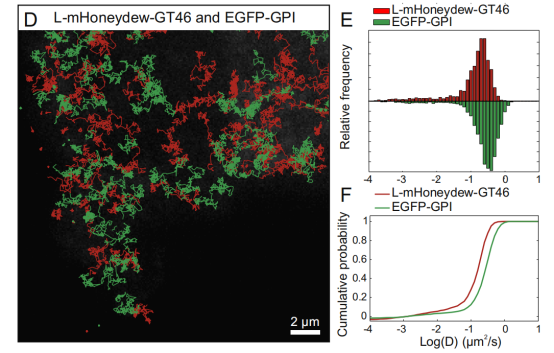
圖7.脂錨定和跨膜分子的膜運動的差異
D.L-mHoneydew-GT46(紅色)和GPI-EGFP(綠色)在基底膜上的運動軌跡。
E.直方圖和F.擴散系數(shù)的累積概率圖。
小結
納米抗體介導的標記提供了一種簡單和通用的方法來標記幾乎任何廣泛可用的GFP和RFP衍生的融合結構,可用于先進的單分子成像應用,包括單顆粒示蹤和單分子定位顯微鏡。由于納米抗體的高親和力和小尺寸,其優(yōu)點包括非常精確和一致的標記,以及在復雜和致密的樣品中具有優(yōu)越的可及性。對于SMLM成像應用,樣品制備非常穩(wěn)健,只涉及幾個簡單的步驟。可在固定后2小時進行成像,縮短實驗周期。同時,納米抗體對固定試劑的選擇、可研究的標本數(shù)量的增加以及圖片切換時所需的還原劑的也不敏感。
此外,使用對抗GFP和RFP的納米抗體,可以用雙色SMLM對任何功能GFP和RFP融合結構的亞細胞進行研究及定位。這使得雙色SMLM成像可以很容易地解決無數(shù)的生物問題。納米抗體在SPT測量中的應用,結合光漂白后的熒光恢復,可以更好地了解質膜中蛋白質的全局和局部方面的運動。
納米抗體相比傳統(tǒng)抗體而言不僅擁有更優(yōu)的理化性質,而且表達和篩選也更加簡便。納米抗體因其小分子,高親和力,高特異性,穩(wěn)定性以及低生產成本等特點在生物學和醫(yī)學領域中實現(xiàn)了多方面的應用。
參考資料:
[1]. Platonova E, Winterflood CM, Junemann A, Albrecht D, Faix J, Ewers H. Single-molecule microscopy of molecules tagged with GFP or RFP derivatives in mammalian cells using nanobody binders. Methods. 2015 Oct 15;88:89-97. doi: 10.1016/j.ymeth.2015.06.018. Epub 2015 Jun 27. PMID: 26123185.
[2]. Albrecht D, Winterflood CM, Ewers H. Dual color single particle tracking via nanobodies. Methods Appl Fluoresc. 2015 Mar 27;3(2):024001. doi: 10.1088/2050-6120/3/2/024001. PMID: 29148490.
了解更多納米抗體相關內容,可關注<阿帕克生物>微信公眾號,獲取最新資訊~
