
前言
噬菌體展示技術(shù)與酵母展示技術(shù)是目前抗體研發(fā)過程中常用的技術(shù),特別是噬菌體展示技術(shù),其對實(shí)驗(yàn)設(shè)備要求很低,常規(guī)分子生物學(xué)實(shí)驗(yàn)室即可開展該實(shí)驗(yàn)技術(shù),加上大容量的文庫庫容,使得該技術(shù)被大家廣泛使用。與之相比,酵母展示技術(shù)雖然發(fā)展了很多年,但是其對設(shè)備要求較高,需要配置流式分選儀,流式分析儀等,加上庫容量有限,所以目前并未被廣泛使用。本文將介紹這兩種技術(shù)的優(yōu)劣勢,以供針對不同靶分子與分子需求時更好地去選擇研發(fā)平臺。
酵母展示技術(shù)是一種廣泛應(yīng)用于研究和工業(yè)生產(chǎn)的通用工具,最早由Maarten P. Schreuder及其同事在1993年報道了酵母細(xì)胞壁外源蛋白的展示,K. Dane Wittrup和同事在1997年報道了酵母表面多肽展示文庫的構(gòu)建和篩選。目前酵母表面展示技術(shù)被廣泛應(yīng)用于蛋白工程,抗體開發(fā),親和力改造等。
酵母展示的原理
釀酒酵母細(xì)胞壁厚且堅硬,約200nm,位于質(zhì)膜外,主要由甘露蛋白和β-鏈葡聚糖組成,具有雙層結(jié)構(gòu),包括內(nèi)部的葡聚糖骨架層,以及主要由甘露蛋白組成的纖維狀或刷子狀外層(圖1)。
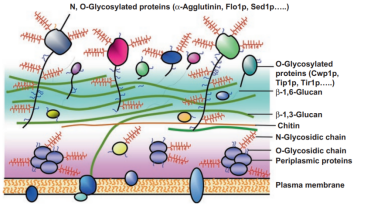
圖1 釀酒酵母細(xì)胞表面結(jié)構(gòu)
通常,目的蛋白的展示通常是通過與宿主酵母細(xì)胞壁蛋白融合表達(dá)而實(shí)現(xiàn)的,常用的錨定蛋白如a-凝集素、Flo1p、Yps1p、Cwp2p、Sed1p、Pir1-4等(圖2)。展示的蛋白經(jīng)分泌途徑,首先被轉(zhuǎn)運(yùn)到內(nèi)質(zhì)網(wǎng)腔內(nèi),然后從內(nèi)質(zhì)網(wǎng)轉(zhuǎn)運(yùn)到高爾基體,最終錨定于細(xì)胞壁表面。常用的錨定蛋白如a-凝集素由Aga1基因編碼的核心亞基和Aga2基因編碼的核心亞基組成,Aga1與Aga2亞基通過二硫鍵相連,并通過AGA1蛋白C端的糖基磷脂酰肌醇(GPI)錨定于細(xì)胞壁。展示的目的蛋白可選擇融合于Aga2亞基的N端或C端進(jìn)行構(gòu)建,納米抗體片段VHH融合于N端或C端均可進(jìn)行高效表達(dá)和篩選。
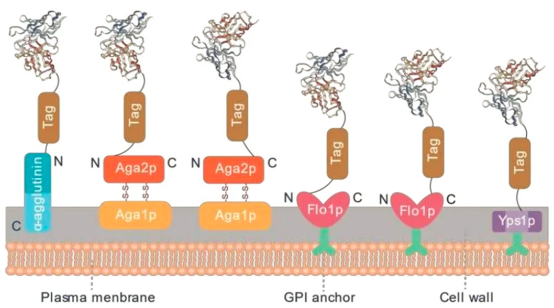
圖2 不同的釀酒酵母細(xì)胞表面展示系統(tǒng)
酵母表面展示主要是通過MACS/FACS來進(jìn)行篩選,篩選過程采用FACS進(jìn)行監(jiān)測,非常直觀與方便。
噬菌體展示的發(fā)展歷史及應(yīng)用概述
噬菌體展示(phage display)是一種利用實(shí)驗(yàn)室進(jìn)化,高通量、高內(nèi)涵地淘選具有特定結(jié)合能力的多肽或抗體的分子生物學(xué)技術(shù),已廣泛用于生物醫(yī)藥、新材料、新能源及環(huán)保相關(guān)的基礎(chǔ)與應(yīng)用研究中。這項(xiàng)技術(shù)最初由George Smith在20世紀(jì)80年代中期開發(fā),并在90年代初由John McCafferty和Gregory Winter應(yīng)用在抗體工程領(lǐng)域。2018年,噬菌體展示研究的兩位先驅(qū),美國科學(xué)家喬治·史密斯(George P. Smith)和英國科學(xué)家格雷格·文特(Gregory P.Winter)榮獲諾貝爾化學(xué)獎。

噬菌體展示的原理
噬菌體展示技術(shù)是將外源的多肽,抗體等片段,插入到噬菌體的結(jié)構(gòu)基因,常見的是與PIII或PVIII融合表達(dá),被展示在噬菌體表面的分子仍然保持生物活性。要從噬菌體文庫中挑選中我們想要的分子,就要經(jīng)過 “淘篩”。該過程簡單地說就是被展示在噬菌體表面的肽庫或者蛋白庫能夠特異地與目標(biāo)抗原識別并結(jié)合,經(jīng)過足夠時間的孵育之后,可使用洗滌液洗去與抗原結(jié)合較弱或者未結(jié)合的游離噬菌體。隨后將特異性結(jié)合的目標(biāo)噬菌體洗脫下來,感染大腸桿菌并進(jìn)行擴(kuò)增以得到下一輪的子噬菌體庫。隨后經(jīng)過2輪~3輪的“吸附-洗脫-擴(kuò)增”富集過程后,能夠與抗原特異性結(jié)合的噬菌體的比例得到了逐步提高。最終獲得能夠識別靶分子的多肽或者蛋白,可被用于后續(xù)的實(shí)驗(yàn)。
Phage display VS Yeast surface display
雖然兩種展示系統(tǒng)都能夠?qū)崿F(xiàn)基因型與表型的統(tǒng)一,且被廣泛應(yīng)用于抗體開發(fā),但是在蛋白表達(dá)系統(tǒng),庫容量,篩選方式等方面,二者存在很大差異。
蛋白表達(dá)系統(tǒng)
噬菌體是一種病毒,需要感染大腸桿菌才能進(jìn)行復(fù)制與擴(kuò)增,是原核表達(dá)體系。但抗體是來源于真核,由于密碼子的偏好性,不能夠讓有些抗體能夠得到有效的展示或有毒,導(dǎo)致克隆丟失。而酵母是真核表達(dá)系統(tǒng),展示的抗體首先轉(zhuǎn)運(yùn)至內(nèi)質(zhì)網(wǎng)腔內(nèi),然后經(jīng)高爾基體進(jìn)行加工,能夠保證蛋白的正確折疊,具有更接近真核表達(dá)蛋白的修飾特征及更良好的生物學(xué)的活性。
庫容量
由于大腸桿菌的轉(zhuǎn)化效率要遠(yuǎn)高于酵母細(xì)胞,一般噬菌體文庫可達(dá)到109。而在很長的一段時間由于技術(shù)的限制,酵母文庫的庫容量只能達(dá)到106~107,因此酵母表面展示一般用于親和力成熟,這種突變文庫,其對庫容量要求不高。納米抗體不涉及傳統(tǒng)抗體輕重鏈體外重組,阿帕克生物經(jīng)過技術(shù)改良目前文庫庫容量能夠保證108,完全能夠滿足納米抗體的研發(fā)需要。
構(gòu)建文庫方式
噬菌體展示文庫采用酶切連接或者同源重組,其中酶切連接的方式大家最常用,相對于體外同源重組成本更低。體外同源重組可以大大提高連接效率,但成本非常高。酵母表面展示是將線性化的目的片段和線性化載體按一定比例電轉(zhuǎn)化酵母感受態(tài)細(xì)胞,片段和載體會在酵母細(xì)胞內(nèi)通過同源重組的方式環(huán)化為質(zhì)粒,成本低廉,操作簡單。
展示效率與拷貝數(shù)
在抗體開發(fā)過程中,噬菌體展示文庫一般采用單價展示,為了達(dá)到單價展示,包裝后展示效率大約10%左右,但是并沒有有效的檢測手段去監(jiān)測文庫的包裝效率,非常讓人頭疼。如果篩選不好,可能是展示效率不好導(dǎo)致的,引入了更多的變量,建議采用抗g3p 抗體,檢測包裝效率。
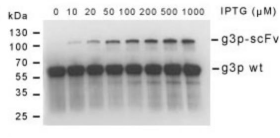
酵母表面展示會帶檢測標(biāo)簽比如HA,F(xiàn)lag,myc等,可以非常方便的通過流式確定文庫表達(dá)效率,一般展示效率可以達(dá)到60%~80%。酵母表面展示是多價展示,一個酵母上大約會有104~105個拷貝。
展示形式
噬菌體展示承載分子量有限一般將多肽,VHH,ScFv或者Fab 融合到PIII蛋白上, Fab片段對噬菌體就相對較大了。 分子量太大,會影響噬菌體的侵染與包裝。然而酵母展示除了可以展示上述的片段外,還可以展示整個抗體IgG分子全長,這是噬菌體展示無法做到。
偏向性
噬菌體的偏向性非常嚴(yán)重,主要是由3個方面引起的:a.噬菌體是原核體系,而抗體來源于真核,由于密碼子的偏好性和有些分子對E.coli有毒,導(dǎo)致克隆生長過程中生長速率不一致,甚至導(dǎo)致克隆丟失;b.沒有插入片段的克隆,生長速度遠(yuǎn)遠(yuǎn)超過插入片段的克隆,導(dǎo)致文庫質(zhì)量降低;c.ORF讀碼框不正確,也會導(dǎo)致這類克隆生長過快。酵母一般不會存在這類問題,生長相對較均一。
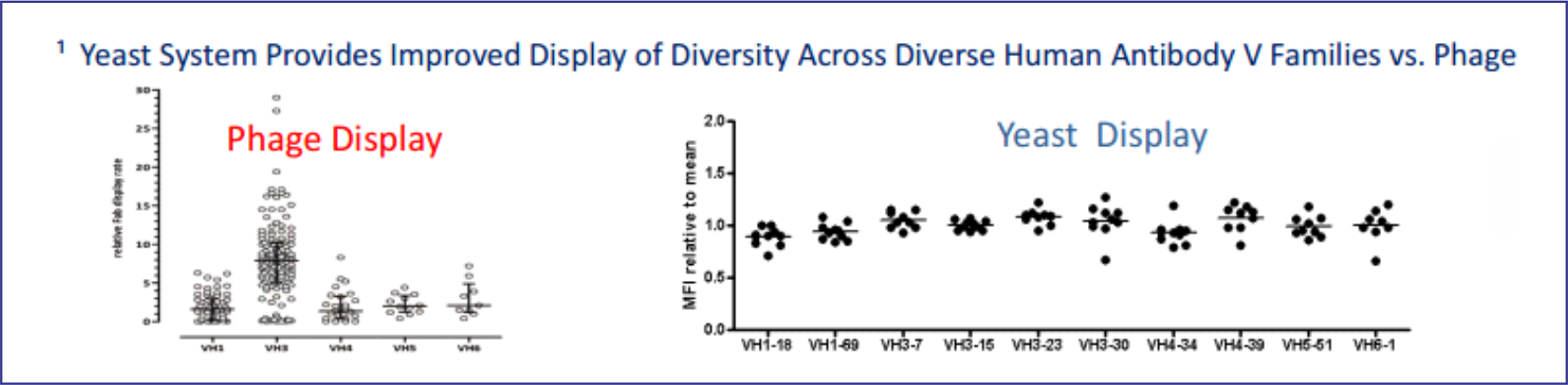
篩選方式
酵母展示最直接的優(yōu)點(diǎn)是在FACS篩選過程中對選擇參數(shù)的精確控制。收集的種群百分比,信號歸一化,和所需的結(jié)合親和力可以通過流式細(xì)胞術(shù)劃定邊界。這種在選擇過程中定義結(jié)合標(biāo)準(zhǔn)的能力比噬菌體展示平臺具有優(yōu)勢,在噬菌體展示平臺上,變異識別依賴于洗滌步驟,而不是實(shí)時動力學(xué)觀察。換句話說,在酵母文庫選擇過程中,這種對理想結(jié)合特性的系統(tǒng)性偏向在噬菌體文庫篩選中是不存在的。酵母表面展示的篩選方法與流式細(xì)胞術(shù)提供的定量和多參數(shù)分析兼容。可對緩沖液組成、pH、溫度和抗原濃度等條件進(jìn)行精確控制,分選在特定孵育條件下與靶蛋白結(jié)合的克隆,如可分選在特定條件下穩(wěn)定性提升的克隆,同時可以逐個分析文庫中的每個細(xì)胞,以實(shí)時了解展示水平及其抗原結(jié)合情況,并分選出特定的細(xì)胞群。我們以實(shí)際案例來展示酵母篩選的優(yōu)勢:
a.基于親和力的分選
噬菌體篩選高親和力克隆是通過增加選擇壓比如包被抗原濃度,洗滌強(qiáng)度等方法,但是卻不能進(jìn)行有效監(jiān)控,同時篩選到的克隆只能區(qū)分陽性,不能分辨親和力高低,只能在蛋白表達(dá)后再做親和力比較,導(dǎo)致工作量大,成本高。酵母展示是通過將待分選文庫經(jīng)不同濃度的靶蛋白孵育后,在一定的靶蛋白孵育濃度下可區(qū)分不同親和力的抗體展示克隆,并按需求進(jìn)行分選。如圖6所示,分選細(xì)胞與不同濃度靶蛋白孵育后的流式圖譜,可觀察到在11.1nM濃度條件下對不同親和力的細(xì)胞群有較明顯的區(qū)分,可以按親和力高、中、低劃分不同分選區(qū)進(jìn)行分選,直接分選高親和力群。這種方式也可以反應(yīng)出文庫中是否有高親和力的群,以及不同親和力群的占比。
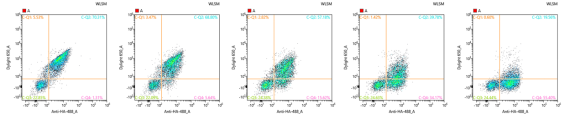
圖6 基于不同親和力的流式分選
(靶蛋白孵育濃度從左至右分別為100nM、33.3nM、11.1nM、3.7nM、1.2nM)
b.Blocking 活性抗體分選
對于免疫檢查點(diǎn)的靶點(diǎn),為了獲得具有生物學(xué)功能的抗體,需要阻斷受體與配體的結(jié)合。常規(guī)的噬菌體篩選是先拿到結(jié)合的抗體,表達(dá)驗(yàn)證后再驗(yàn)證是否能blocking 受體與配合的結(jié)合,效率低,成功率不高。酵母表面展示是通過對配體蛋白或bench mark抗體進(jìn)行染色標(biāo)記,通過競爭分選來獲得。如分選PD-L1的阻斷抗體,將PD-L1和PD-1標(biāo)記為不同的熒光,與文庫細(xì)胞共孵育后分選表達(dá)信號陽克隆中PD-L1熒光信號陽而PD-1信號陰的克隆,見圖7所示分選圖譜,分選F-Q1區(qū)細(xì)胞,經(jīng)鑒定細(xì)胞結(jié)合PD-L1后不再結(jié)合PD-1,即抗體具有阻斷PD-L1與PD-1結(jié)合的功能,效率非常高。
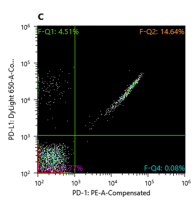
(1)
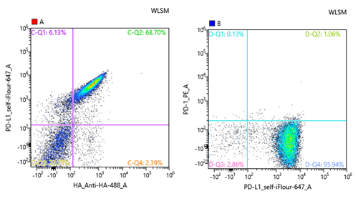
(2)
圖7 特定表位分選及鑒定圖譜(1:PD-L1標(biāo)記熒光650,PD-1標(biāo)記熒光PE,分選650信號陽性且PE信號陰性的區(qū)域F-Q1;2:分選產(chǎn)物流式鑒定圖譜,左信號PD-L1-647/HA-488,右信號PD-1-PE/PD-L1-647)
out put 克隆陽性率與數(shù)據(jù)分析深度
噬菌體的篩選類似于ELISA,一般會通過2~3輪的panning,這個過程為了保證克隆的多樣性,應(yīng)盡量減少淘洗的輪次,不要讓output陽性率太高。其次絲狀噬菌體比較黏,容易出現(xiàn)非特異,酵母則是通過檢測表達(dá)標(biāo)簽與抗原結(jié)合雙陽信號來控制,非特異非常低。酵母展示一般第一輪進(jìn)行MACS富集,第二輪采用FACS進(jìn)行分選,直接分選特定群,通過控制分選精度,可以讓陽性率達(dá)到90%以上,且不丟失多樣性。傳統(tǒng)的克隆分析是通過挑取單克隆來進(jìn)行驗(yàn)證與sanger測序,一般挑取5~10塊板,這種方式往往挑選到的都是豐度比較高的克隆,對于低豐度的克隆,很難通過這種方式獲得,數(shù)據(jù)量有限。酵母展示除了這種挑單克隆的方式來獲得克隆外,阿帕克生物采用分選特定群10w+的陽性克隆,進(jìn)行NGS測序,分析深度是傳統(tǒng)挑克隆無法比擬的,獲得的數(shù)據(jù)可以進(jìn)行豐度排序,或者基于CDR3進(jìn)行cluster聚類,輕松獲得上百條后選克隆。噬菌體由于比較黏且容易非特異,NGS測序的結(jié)果陽性克隆的置信度非常低,往往我們合成的克隆沒有幾個是陽性。
了解更多納米抗體相關(guān)內(nèi)容,可關(guān)注<阿帕克生物>微信公眾號,獲取最新資訊~


